��������
��ϵ����
�㽭��Դ��Ʒ����Ƽ�����˾
�绰��0570��8788056
���棺0570��8788381
���䣺zjgykp@163.com
��ַ���㽭ʡ�����ж��۾��ÿ�����
����4·2��
- ���Թ����Ŀ����������о���չ
- ����ʱ�䣺 2019-05-07�����������6081��
���Թ����Ŀ����������о���չ
���IJ� 1������ 1��Ԭѩ�� 2�������� 1,*
(1.����ҽѧԺ������ѧ����ѧԺ˗2.����ҽѧԺ��������ѧԺ������ ���� 453003)
ժҪ��������һ���Ծ۰�����ȩ��Ϊ�Ǽܡ����������Ƿ�֧�ṹ��ֲ���Ӷ��ǡ�ͨ�������ֶζԹ������и��ԣ�������������������ȡ��ށ����۽ṹ��������������öȣ������������������յ���������ǿ����ϸ���Ի���ҩ��������ԡ���������Ѫ��������ת�Ʋ���ǿ������Ӧ�������ص������˸��Թ����Ŀ��������ơ����ջ��ƺͿ�������Ч��ϵ����չ���˽��俪��ΪʳƷ��ǰ����
�ؼ���˖������������-3�����Թ���������ᶥ���ٹ�����������������
������һ�ִ�����ֲ��㒚���ڵĸ��Ӷ��ǣ�������ʳƷ���Ӽ���ҩ�︨��[1]ͨ����ѧ�Լ�[2-3]ǃ��[4-5]ǃ����[6]��ø����[7]���ܽ������������������ȣ����ށ����۽ṹ������߿��������Եĸ��Թ���(modified pectin, MPs)���� pH ���Ը��ٹ���(pH-modified citrus pectin, MCP)��������������ǃ��������Ѫ������ǃ������ת��(metastasis)�ȷ�����л��ԡ������� MCP Ϊ�������ܽ� MPs �Ľṹ�����������Ի��ƺ�Ч��ϵ(structure-activity relationship, SAR)��
1 �����ṹ��Ȼ����һ�㺬��ͬ�۰�����ȩ��(homogalacturonan, HG) . �����ǰ�����ȩ����� I (rhamnogalacturonan-I, RG-I)��ȡ��������ȩ�����(substituted galacturonans, GS)[8-10]�������ṹ����Դ.��ȡ���յ����ػ��ϴ�ͨ�� HG Լռ 65%��RG-I ռ 20~35%������ΪGS���ٹ���(citrus pectin, CP)�е� RG-I ����Զ���� RG-II [11]��HG ����D-������ȩ��(D-galacturonic acid, GalpA)����-1, 4 ���ռ����ӵ�ֱ�����ӡ���ҵ��Դ�� CP ��HG ���ֵij��ȴ�ԼΪ20 kD [12]������ GalpA �� C-6 λ�Ȼ��������̶�(degree of methylation, DM)��������ɷ�Ϊ���������͵������������ǵ����ʲ��ܴ�RG-I�����������ǺͰ�����ȩ����ɵĺ����ظ�Ƭ��„[(��4)-��-D-GalpA-(1��2)-��-L-Rhap-(1��)]noRG-I ��GalpA һ�㲻��������֧����Լ 20~80%�����ǵ� C-4 �ǻ������ж��ֽṹ�����֧������ֲ����Դ�IJ�����Ҫ�����������͵�Ƭ��„����-(1,4)�����ӵĹѾ۰����ǣ�I �Ͱ������������(type I arabinogalactan, AG-I)�� II �Ͱ������������(type II arabinogalactan, AG-II)���������͡�CP ��RG-I��Ҫ�ɹѾ۰����� AG-I ��ɣ�AG-I ����-(1,4)������-(1,3)�����ӵ����ְ���Ѿ�����ɡ�L-�������dz�������-(1,5)�����ӵ���-(1,4)����ɵİ���Ѿ��ǵ��м��ĩ��[13-14]��RG-II ����Ҫ��GS������ṹ������RG-I ����ϴ�������ΪHG �ṹ������ A �� B ����������MPs �Ľṹ���������һ�£���Ҫ����HG ������ RG-I ֧�������������������ȸ���.��֧����[10]��
1 ���Թ����Ŀ��������Լ�����
MCP ��������������.Ѫ��������ת�Ƶȶ�������ã�������ǰ���ٰ��ķ�ת��[4].��ɫ�����ķ�ת��[3].�᳦���ĸ�ת��[15].���ٰ�[16]��Ѫ��������[17]���俹���������漰����������������. �Ի���ҩ�������.��ת�Ƶ����ƺͶ�����ϸ���ĵ��صȣ�ͼһ����
2.1 ���Թ�����������������������
MCP �ȸ��Թ��������ƶ�������ʵ����[3,16,18-19]���������ÿ����漰��������[20-21].����ϸ����ֳ.����;���ȡ�MCP �п���ͨ�����������ڰе������������-3(galectin-3, Gal-3)��𤵰��MUC2 ��ص����ö����ƽ᳦���ķ�����ת��:�п���������LPS/TLR4/NF-��B ;���շ��᳦��ת���᳦��[20]:������ͨ��Ӱ������ϸ�����ڶ�������ֳ[22-23]��MCP ���������������ƿ�����Gal-3 ���Ƶ����������ź�;��(����MAPK ;��.Wnt ;��)[24-26]�͵���;���й�[27]����������ͬ����MPs ������ϸ�����������ò���һ�£���������Է���.�ṹ�����й�[4]������ϸ����������Ҳ����ɿ��������Բ�һ�µ�ԭ��֮һ��
2.2 ���Թ����Ի���ҩ�����������
�����������ܹ�ʹijЩ�Ի���ҩ����ڿ��Ե�����ϸ���ܹ���������[28-31]��Chauhan ��[32]���ָ����ٹ���GCS-100 ���յ��Ե�������.�����ػ�ù���п��Ե������Թ�����ϸ��ϵ�ĵ������ڻ���ʱʹ�ø��Թ������������ٴ�L�����ж��Ļ���ҩ��������ӻ�������ҩ�Եķ����������Ļ����������Կ���ͨ������ Gal-3 ����ת������ҩ��[33]������������Gal-3 ��TRAIL �� DR4/DR5 ��������й�[34]��ʹ����ϸ���Ի���ҩ���ɲ����б�Ϊ���С�
2.3 ���Թ�����ת�Ƶ�����
MPs ��ͨ������ Gal-3 ����������Ѫ������.ʧ����������.Ѫ����Ƥϸ��𤸽��ת�ƹ���[16,35-37]��ѪҺѭ���������Gal-3 ������ת���йأ���������ѪҺ��������������Gal-3 ������ת����صĹ���[36]�����⣬Gal-3 ���µ�G1-S ��㒚��������ˮƽ(cyclin E �� cyclin A)��L��������Ƶ���(p21WAF1 �� p27KIP1)ˮƽ��ʹ����������[38-39]�����⣬�˲ι���������������ϸ��Ǩ�Ƶ�������ʹ���п�ת��DZ��[40]��
2.4 ���Թ���������ϸ��������
MPs����Ϊ���ߵ��ڼ�(biological response modifiers, BRMs)��������ϸ��[41]��MCP��������͵�Tc, B, NK ������ϸ�����ߴ̼���Щϸ���ͷ� INF-�õ�ϸ������[42-43]������Gal-3 ������Jurkat Tϸ���������������䷢������[44-45]�����⣬��� MPs ������Gal-3�յ���Tϸ��������߭�п�����ǿ�������������á�
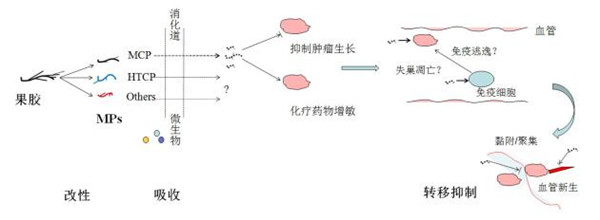
ͼ 1 ���Թ������û���ʾ��ͼ
Fig. 1 Schematic diagram of antitumor mechanisms for MPs.
3 MCP ���ԵĻ���������������
��MCP Ϊ������MPs �������ڷ��ӿ��������Ե�ǰ���ǽ���ѪҺѭ�����������������ö�[10,16]��ΪʲôCP û����������ת�ƵĻ��ԣ���MCP������һ���ԣ����ȣ�ˮ��ʹ�������ӵ��������ʷ��������ܽ�����ӡ���ʹ CP �Ǽ� HG ͨ����-�������ö����̣������ȴӴ�Լ 80%������10%���£� �ܽ�����ӡ���Σ����ӵġ�ҩЧ���š�������ֲ�״̬��ˮ������з����ı䡣������Ǽ�����ռ�������ǵ����ռ���������У���������� RG-I ��ľ�Ѿ���.�������Ѿ��ǵ�Ƭ�ε�����ʴ��ڰ���Ѿ���Ƭ�Σ���ʹ�ù����ĹǼܺ�ë�����������̣����ְ���������Ѿ����еİ������DZ�ˮ�⣬����Ѿ��DZ��������Ӷ���ǿ����ν��ҩЧ���š�ĩ����-������������е� Gal-3 ����ʶ��ṹ��������[46-47]������������ˮ�г���ˮ�ž��������״̬���� MCP �����ǿ��ܵģ���ĩ����-�����Dzл����ڡ����֡����з��� Gal-3����һ��Ӱ��MCP ҩ������ѧ���ʵIJ����Ƿ�������MCP ��������3000~60 000 ��Χ֮�� [10,13,42]�����Ӵ�С���ܴ����պ����������������ѪҩŨ�ȡ�
MPs �������öȵĸߵ������������ʺ����ջ����йء���ɿ����Ǿ������������յ���Ҫ���ء� ����Caco-2 ˫��ϸ��ģ�Ͷ� MCP �Ŀ�Ĥ���ս��е��о�������������й��������Թ���Ƭ�δ�Խ��Ĥ�������а�����ȩ��Ĺ���Ƭ��û����Ĥ[48]��MPs������ͨ���������ջ���������(��ͨ��С��LƤϸ��.������ܰ���֯.Mϸ�����յ�)���ַ�ʽ������.ת�˺��ͷ�[49-50]��
4 ��Ч��ϵ
SAR �о�������ָ�����ӽṹ�Ż�������ԡ�Ȼ�������ڹ����ṹ�dz����ӣ�MPs ��Ȼ�����˳��������ͷ��飬�����������Dz���һ�ġ����磬����Ƭ�κ�����Ƭ�ξ��в�ͬ�����ʣ���Gao ��[13]��������DEAE ��ά�ز�������MCP ������Ƭ��MCP-N ������������ˣ����ǵ�SAR ��Ϊ����Ч��ϵ��������Ϊȷ�С�����MPs ��SAR ��Ҫ�Ʊ����ṹ����һ�µĹ���Ƭ�Ρ�
MPs ������RG-I �İ�����ĩ�˺�������ṹ�ǿ��������ԵĹؼ�����[13, 51]��ӫ������.��ʽϸ���Ǻ�ԭ�����羵������֤ʵ�������İ���Ѿ���ĩ���ܹ���Gal-3 ����[51]����-D-���۰�������Gal-3 ��Ľ��볣��Ϊ 0.33 s-1 [52]�����������[53]������������[54]���нϸ߱�����RG-I Ƭ�Σ����Ǿ�
���п��������ԡ�Gao ��[13]�Ʊ���MCP-N ���ڹ�����AG-I ��Ƭ�Ρ����ǽ�MCP-N ����-L-�����������ø�������õ����Թ���Ƭ��M-MCP��M-MCP ��һ�ַ�����ԼΪ18 kDa �ľ�����-1, 4 ���ռ��İ���Ѿ���Ƭ�Ρ����ή��M-MCP �õ��İ���Ѿ��DZ�AG-I ���͵Ĺ���Ƭ�ξ��и�ǿ��Gal-3 ���ƻ��ԡ�
HG �Կ���������Ҳ���ڹ��ס����ȣ�HG ����������ϸ��Ǩ�ƻ����йء�Fan ��[40]���֣��˲ι�����L-929 ϸ��Ǩ�Ƶ�������HG ��أ�������RG-I �ء���Σ�HG ����������յ������йء�ͨ����CP �ȴ������HTCP��ʹHG ���������յ����ԣ�������Ȼ�����в����ڵĽṹ[4]�����⣬MCP���߱��յ������Ļ��ԡ�HG ������-�������Ի�����������Dzл��������Dzл������� MCP �յ�NKϸ���Ļ����й�[42]�������ȴ����������ᾭ��-�����������л�ԭ�ԵIJ������Dzл�.�������Ż����������ṹ������Ƭ�Ρ�MPs ������ʹ����ϸ������ʧ������[55]���û����������RG-I ����HG��أ�Ŀǰ������[4,54]�����⣬HG ���ܲ��� Gal-3 �ķ�������ʶ�𡣾���Gal-3 ͨ��CRD KҪ����Թ����İ���Ѿ��Ƿ���רһ������ã����ǣ�HG �Ǽܶ�����Gal-3 ���Բ��Ǻ�����[56]�����������в�����֧�ֽ���RG-I �ṹfl���������й�[6,54,57]��Gao ��[13]�����Ƿ����GalpA��ɫ������MCP ����Ϊ�������GalpA �����Ϊ MCP-A������ GalpA �����Ϊ MCP-N��ǰ�߶� Gal-3 ������ԶԶ���ں��ߡ�����Ƭ�κ��� GalpA �ĹǼܶ���ά�ְ���Ѿ���ĩ��Ƭ�εĹ����й��ס��ֲ���HG�Ǽ�L�Ķ������Ѿ����ܹ���Gal-3 ����Эͬ�����[56]���������������ؼ�����������ЧӦ(multivalent effect or glycocluster effect)���������ǿ�Ƚ����ӡ� ���Թ���L HG �Ǽܣ�������Щ����Ѿ���������ԣ����š������á�Gao ��[56]�۲쵽�˼������������ǵĹ����Ǽ���Gal-3�������ã�����������ò������ǵ����ơ���ˣ����Թ����ĹǼ��п����� CRD ֮�䷢����רһ������á�
MPs �������Dzл������簢�����ǻ������Բ���Ӱ�졣Gao ��[56]�۲쵽�������Ǽȿ�������Ҳ���Լ��ٰ���Ѿ���Ƭ���� Gal-3 �������á�����������������ĵ����ڶ����Dzл���Ӱ����ʶ��רһ��[58]������������ʮ���ְ����������أ������������ĩ���Dzл��ṹ���о��DZ�Ҫ�ġ��о����Թ����Ŀ����� SAR.��л����ѧ���������ƶ�ɸѡ�����Ľ������Ի�����ܸ��ŵİ��������������������Ƽ�(galectin-3 inhibitor, Gal3I)��Gal-3 ��Ϊ�����е�Խ��Խ���˹�ע��Ŀǰ�Ѿ�����������Gal3I[59-60]��Gal3I �������������Ʒ������ž�Ӧ��DZ�������ڰ� Gal-3 ���ԣ����������Ƽ�������ֻ���Ը��Թ���Ϊ�ȵ�������һ��·�������ܵ������������ս�����о���ѧ�ϳɵ�Gal3I �����У���������� Gal-3 �� CRD fl���������õĹ��ɡ���Щ���ɶ����Ż��Ը��Թ���Ϊ�ȵ����ӵ� Gal3I �Ľṹ�����а��������ڻ�ѧ�ϳɵ� Gal3I ������ѧ�о��������flֲ��.������ʳ����Դ��ɸѡGal3I ���о��Ѿ��㷺��չ[59, 61]��Ŀǰ����ȱ��һ�㷺�Ͽɵ�.��ͨ���� Gal-3I ɸѡ���������ڸ��Թ����м��������� Gal-3I �Ŀ���ɸѡ�����Ը���.���Ը�С��Ƭ�Ρ�
4 չ��
����MPs������������ת��.���ƻ���Ч������ǿ������Ӧ�Ļ��ԣ�������� MPs Ϊ����������ʳƷDZ����MPs �Ļ��Կ�������RG-I Ƭ���йأ�ͬʱ���������ö�Ҳ��Ӱ����ԡ�����MPs��SAR��ָ���ṹ�Ż���������ɸѡ��������֡�Ϊ�˽� MPs ����Ϊ����ʳƷ��Ӧ�ص������о�������е��ҩ�й�ϵ.��ø����ҩЧѧ.ҩ��ѧ�Լ��ٴ��о����ݡ����⣬һЩ�������û��ƺ��������ö��йصĻ���������ҲӦ���������磬�о����ֵͷ������Ĺ������п���������[62]���������Ŀ����������뿹��������֮���Ƿ���������ϵ[6]�������ܹ���ϸ�����ӷ�������ã�MPs�Ƿ������ϸ�����ӷ������ã�����Ӱ������������[63]�����ڵ������ȵĹ����ܹ�����һЩ�������ӣ����Թ����������Ƿ��Կ��������ҩ�����Ӱ�죿MPs ����ܵ�������Ⱥ��Ӱ�죿���ͺ��������������Ӱ�����������öȣ����մٽ����ܷ����� MPs ���������öȣ�������Щ���⣬�������ڸ��� MPs ���Բ��ٽ����г�Ӧ�á�
�ο����ף�
[1] WICKER L, KIM Y, KIM MJ, et al. Pectin as a bioactive polysaccharide �C Extracting tailored function from less[J]. Food Hydrocolloids, 2014, 42(2): 251-259.
[2] ALMEIDA EA, FACCHI SP, MARTINS AF, et al. Synthesis and characterization of pectin derivative with antitumor property against Caco-2 colon cancer cells[J]. Carbohydrate Polymers, 2015, 115: 139-145.
[3] PLATT D, RAZ A. Modulation of the lung colonization of B16-F1 melanoma cells by citrus pectin[J]. Journal of the National Cancer Institute, 1992, 84(6): 438-442.
[4] JACKSON CL, DREADEN TM, THEOBALD LK, et al. Pectin induces apoptosis in human prostate cancer cells: Correlation of apoptotic function with pectin structure[J]. Glycobiology, 2007, 17(8): 805-819.
[5] HAO M, YUAN X, CHENG H, et al. Comparative studies on the anti-tumor activities of high temperature- and pH-modified citrus pectins[J]. Food & Function, 2013, 4(6): 960-971.
[6] KANG HJ, JO C, KWON JH, et al. Antioxidant and cancer cell proliferation inhibition effect of citrus pectin-oligosaccharide prepared by irradiation[J]. Journal of Medicinal Food, 2006, 9(3): 313-320.
[7] OLANO-MARTIN E, GIBSON GR, RASTELL RA. Comparison of the in vitro bifidogenic properties of pectins and pectic-oligosaccharides[J]. Journal of Applied Microbiology, 2002, 93: 505�C511.
[8] CAFFALL KH, MOHNEN D. The structure, function, and biosynthesis of plant cell wall pectic polysaccharides[J].Carbohydrate Research, 344(14): 1879-1900.
[9] LECLERE L, CUTSEM PV, MICHIELS. Anti-cancer activities of pH- or heat-modified pectin[J].2013, 4, 128: 1-8. eCollection.
[10] ���IJ�, ߬����, ����. ���� �ٹ������Ʊ�, ��������������[J]. �ߵ�ѧУ��ѧѧ��, 2010, 31(5): 964-969.
[11] MOHNEN D. Pectin structure and biosynthesis[J]. Current Opinion in Plant Biology, 2008, 11(3): 266-277.
[12] YAPO BM, LEROUGE P, THIBAULT JF, et al.Pectins from citrus peel cell walls contain homogalacturonans homogenous with respect to molar mass, rhamnogalacturonan I and rhamnogalacturonan II[J]. Carbohydrate Polymers, 2007, 69(3): 426�C435.
[13] GAO X, ZHI Y, ZHANG T, et al. Analysis of the neutral polysaccharide fraction of MCP and its inhibitory activity on galectin-3[J]. Glycoconjugate Journal, 2012, 29(4): 159-165.
[14] HINZ SW, VERHOEF R, SCHOLS HA, et al. Type I arabinogalactan contains ��-D-Galp-(1-->3)-��-D-Galp structural elements[J]. Carbohydrate Research, 2005, 340(13): 2135-2143.
[15] LIU HY, HUANG ZL, YANG GH, et al. Inhibitory effect of modified citrus pectin on liver metastases in a mouse colon cancer
Progress in Anti-tumor Mechanisms of Modified Pectin
ZHANG Wen-bo1, LIU Zhen-hua1, YUAN Xue-yan2, GAO Qi-yu1,∗
(1. School of Life Sciences & Technology, Xinxiang Medical University;
2. School of Public Health, Xinxiang Medical University, Xinxiang Henan 453003, China)
Abstract: Pectin is a complex class of plant polysaccharides, composing galacturonan backbone and neutral sugar side chains. Antitumor modified pectin fragments (MPs) can be prepared by physical and/or chemical modification to decrease its molecular weight, reduce its degrees of esterification, modify its fine structure and improve its bioavailability. It was reported that MPs could inhibit tumor growth, induce apoptosis, sensitize tumor cell to chemotherapy drug, interfere angiogenesis, suppress metastasis and modulate immunological responses. In this review article, we will summarize the antitumor mechanisms, bio-absorption mechanism and structure-activity relationship of MPs. We also analyze the prospects for developing MPs into functional foods.
Key words: galectin-3 (Gal-3); modified pectin (MPs); modified citrus pectin (MCP); pectin; antitumorInitially, pectin can be modified into MPs using different methods, such as acid/base treatment and heat-treatment. Then, MPs, including MCP, HTCP and/or other modified pectin fragments can be absorbed partly by the gastrointestinal tract. Also, they may be degraded by the gut microbiota as dietary fiber and then absorbed by the body. Bioavailable MPs can probably inhibit tumor growth through modulating cell cycle or apoptosis pathway by binding Gal-3 in vivo. Additionally, MPs can facilitate chemo-therapy to some extent. It is speculated that MPs may be helpful for inducing cell death for those suffering from anoikis-resistance or immune escape. Last but not least, MPs can block tumor cell aggregation, inhibit angiogenesis and preclude tumor cell from lodging to the distant target organ, which is helpful for suppressing metastasis.
- ��һƪ�������Ŀ����������о���չ
��һƪ���ͷ��Ӹ��ٹ��������������е��о���չ - ���������б�

